
Создание биологического водителя ритма сердца
| Категория реферата: Рефераты по медицине
| Теги реферата: контрольные 9 класс, allbest
| Добавил(а) на сайт: Глен.
Предыдущая страница реферата | 1 2 3 | Следующая страница реферата
Когда выяснилось, что определенные подтипы эмбриональных стволовых клеток генерируют импульсы, сходные со спонтанными импульсами истинных водителей ритма, попытались использовать эти клетки в качестве биологических пейсмекеров [22]. Но и здесь возникло немало проблем.
Во-первых, поскольку незрелые эмбриональные стволовые клетки после прекращения дифференцировки могут утратить пейсмекерные характеристики, было бы большим достижением, если бы удалось останавить развитие полученных кардиомиоцитов на стадии сино-атриальных клеток.
Во-вторых, важно выяснить, какие каналы определяют спонтанный ритм пересаженных клеток, и убедиться, что это именно те каналы, которые обеспечивают работу истинных водителей ритма в сердце человека. Кроме того, надо знать, как созданная конструкция будет отвечать на стимуляцию вегетативных нервов, т.е. определить чувствительность новых кардиомиоцитов к автономным нервным воздействиям. Эти вопросы возникли в связи с потенциальной аритмогенностью создаваемых водителей ритма [23]. Ответив на эти вопросы, можно понять: развитие аритмии в данном случае - артефакт (например, следствие экспериментальных манипуляций) или потенциально опасное свойство биологических пейсмекеров, созданных на основе эмбриональных стволовых клеток. И наконец, не решена проблема иммунного ответа организма на присутствие завершивших дифференцировку клеток. В этом отношении более перспективны, на наш взгляд, мезенхимальные стволовые клетки, которые, как и эмбриональные, полипотентны (т.е. способны дифференцироваться в ряд клеточных линий, включая клетки скелетных мышц и клетки соединительной ткани), но при этом, по-видимому, обладают “иммунопривилегированностью” - на последних стадиях развития не вызывают существенного иммунного ответа [24].
Изначально стволовые клетки были обнаружены в костном мозге взрослого организма (точнее, в мезенхиме, или строме, костного мозга). Впоследствии оказалось, что они присутствуют практически во всех органах взрослых животных и человека; тем не менее обычно их выделяют из костного мозга. Таким образом, появилась заманчивая перспектива: создание банка мезенхимальных стволовых клеток для клеточной терапии различных патологий. В случае, когда по каким-либо причинам нельзя использовать донорские стволовые клетки, их источником может служить собственный костный мозг пациента. Однако до того как это будет введено в практику, необходимо более тщательно изучить биобезопасность, в частности “иммунопривилегированность”, стволовых клеток.
Мы рассматривали мезенхимальные стволовые клетки взрослого человека в качестве основного экспериментального материала. Прежде всего нас привлекли стабильность клеточных линий и их низкая антигенность. Однако мезенхимальные стволовые клетки человека не способны генерировать пейсмекерный ток If, поэтому необходимо было нагрузить их геном HCN2, который, напомню, отвечает за трансляцию синтеза белков, формирующих и переносящих If. Сделано это было с помощью метода электропорации: клетки поместили в пульсирующее электрическое поле, благодаря чему временно открывались поры в клеточной мембране, через которые мог проникнуть вирусный переносчик со встроенным геном HCN2; при этом эффективность заражения составляла 35-45% [25].
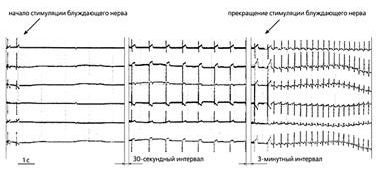
Рис.3. ЭКГ собаки спустя пять дней после имплантации мезенхимальных стволовых клеток человека, содержащих гены GFP и HCN2, в эпикард ее левого желудочка [26]. Слева направо: синусовый ритм до и после начала стимуляции блуждающего нерва, идиовентрикулярный ритм во время вагусной стимуляции и восстановление синусового ритма после прекращения стимуляции блуждающего нерва.
Модифицированные человеческие стволовые клетки с экспрессированным геном HCN2 были пересажены в небольшую область эпикарда левого желудочка собак [25]. Через неделю у них на фоне угнетения ритма сино-атриального узла развились ритмы ускользания с частотой 60 возбуждений в минуту (рис.3). Локализация источника ритма в месте имплантации стволовых клеток определялась с помощью метода флуоресцентного оптического картирования *.
* “Оптические измерения трансмембранного потенциала были задуманы американским исследователем Л.Коэном. Идея основана на свойствах специально синтезированных молекул-флуорофоров, которые, связавшись с клеточной мембраной, способны поглощать и излучать свет с эффективностью, зависящей от величины электрического поля, в котором находится эта молекула. Таким образом, осветив сердце, прокрашенное флуорофором, можно оптически измерить кинетику трансмембранного потенциала по изменениям интенсивности или длины волны флуоресценции. Более того, используя современные методы двухмерной регистрации света, можно составлять карты изменения трансмембранного потенциала на поверхности сердца. Оптическая природа измерений позволяет изменять пространственное разрешение картирования сигналов путем простой замены оптического увеличения. В настоящее время картирование трансмембранного потенциала осуществляется в широком диапазоне пространственного масштаба: от единичной клетки до целого сердца”. (Ефимов И.Р., Самбелашвили А.Т., Никольский В.Н. // Вестник аритмии. 2002. №26. С.91-96.) - Примеч.ред.
Гистологические исследования показали, что пересаженные в миокард собаки мезенхимальные стволовые клетки человека сформировали между собой и с желудочковыми миоцитами так называемые щелевые контакты - канальные белки, переносящие электрический ток между сопряженными клетками (рис.4) [26]. Полученный пейсмекерный ток проявлял типичные для него свойства: активизировался при гиперполяризации клетки, отвечал на катехоламины и ацетилхолин и блокировался цезием [25].
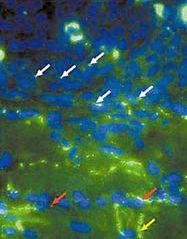
Рис. 4. Микрофотография гистологического среза миокарда собаки, которой имплантировали человеческие стволовых клеток с экспрессированным геном HCN2 [26]. Белыми стрелками показаны щелевые контакты, образовавшиеся между стволовыми клетками, красными - между стволовыми клетками и кардиомиоцитами, фиолетовой стрелкой отмечено место пролиферации стволовых клеток (интеркалярный, или вставочный диск).
Итак, мезенхимальные стволовые клетки взрослого человека, судя по всему, можно использовать в качестве субстрата для формирования сино-атриального узла, что было подтверждено в экспериментах на собаках. Но прежде, чем дойдет очередь до человека, предстоит сделать еще очень многое. Например, проверить in situ чувствительность биологического водителя ритма к автономным нервным воздействиям, сравнить длительность функции созданного биологического пейсмекера и его эффективность с соответствующими параметрами электрокардиостимулятора, проверить на токсичность и тератогенность. Кроме того, выяснить, задержатся ли используемые генные конструкции и клетки именно там, куда их ввели, или мигрируют. Неизвестно также, останутся ли стволовые клетки после трансплантации дискретными и/или дифференцируются в другие клеточные типы, и не будут ли они отторгаться. И наконец, надо устранить главный недостаток биологических пейсмекеров, проявившийся как в экспериментах с использованием аденовирусных конструкций, так и стволовых клеток, несущих ген HCN2, - сократить интервал между остановкой синусового ритма и до возникновения идиовентрикулярного (в идеале он должен длиться одну-две секунды).
До тех пор, пока не удастся ответить на все эти вопросы, рано говорить о практическом применении биологических водителей ритма и отказываться от электронных пейсмекеров - главного достижения 20-го столетия в лечении заболеваний проводящей системы сердца. Тем не менее есть все основания надеяться, что не за горами то время, когда с помощью генной и клеточной терапии будут решаться многие проблемы в различных областях медицины, и только наше воображение может ограничить применение этих методик.
Работа выполнена при поддержке USPHS-NHLBI (проекты № HL-28958, HL-67101, HL-20559, GM-55263) и отмечена премией “Heritage”, учрежденной Американской ассоциацией сердца (American Heart Association).
Список литературы
1. Zivin A., Bardy G.H. Cardiac pacemakers // Foundations of Cardiac Arrhythmias / Eds. P.M.Spooner, M.R.Rosen. N.Y., 2001. P.571-598.
2. Hoffman B.F., Cranefield P.F. Electrophysiology of the Heart. N.Y., 1960.
3. DiFrancesco D. // J. Physiol. 1981. №314. P.377-393.
4. DiFrancesco D. // J. Physiol. 1982. №329. P.485-507.
5. Brown H.F., Kimura J., Noble D. // Proc. R. Soc. Lond. B. 1984. №222. P.329-347.
6. Hagiwara N., Irisawa H., Kameyama M. // J. Physiol (Lond). 1988. №395. P.233-253.
7. Hagiwara N., Irisawa H., Kasanuki H. // J. Physiol (Lond). 1992. №448. P.53-72.
8. Noma A., Irisawa H. // Jpn J. Physiol. 1975. №25. P.287-302.
9. Ono K., Ito H. // Am. J. Physiol. 1995. №269. P.H453-H462.
Рекомендуем скачать другие рефераты по теме: бесплатные курсовые работы скачать, рассказы скачать.
Категории:
Предыдущая страница реферата | 1 2 3 | Следующая страница реферата
 Главная
Главная