Известно, что
соединение водорода с кислородом происходит в большинстве случаев с взрывом, но
причина этого до сих пор не известна. Попытаемся найти её.
Энергия синтеза
молекулы водорода равна 436кДж/моль или 4,53эВ на одну молекулу. Поскольку
молекула состоит из двух атомов, то указанная энергия распределяется между
ними. Таким образом, энергия одной связи между атомами водорода оказывается
равной 2,26эВ (рис.4). При механическом разрыве этой достаточно затратить
2,26эВ. При термическом разрушении этой связи энергии потребуется в два раза
больше (2,26×2=4,53эВ).
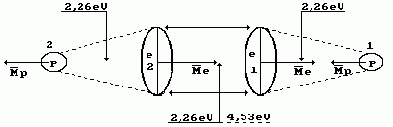
Рис. 4.
Молекула водорода
Для образования
двух молекул воды необходимо разрушить на атомы две молекулы водорода и одну
молекулу кислорода. При механическом разрушении ковалентных связей на
разрушение двух молекул водорода затрачивается 2,26×2=4,53эВ, а молекулы
кислорода – 2,56эВ. Сумма этих энергий равна 7,13эВ. Если процессы разрушения
указанных молекул проводить термическим путем, то на разрушение двух молекул
водорода потребуется 4,53+4,53=9,06эВ, а на разрушение одной молекулы кислорода
– 5,13эВ. В сумме это составит 14,19эВ. Разница почти двукратная.
Известно, что
при синтезе одного моля воды выделяется 285,8кДж или 285,8·1000/6,02·1023·1,6·10–19=2,9эВ
на одну молекулу. Так как молекула воды состоит из одного атома кислорода и
двух атомов водорода, то на одну связь приходится 2,96/2=1,48эВ (рис.5). Из
этого следует, что электроны атомов водорода и кислорода в молекуле воды
находятся при обычной температуре (1,48/2=0,74эВ) между четвертыми и пятыми
энергетическими уровнями (табл.1,2).
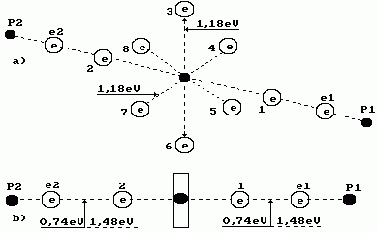
Рис. 5. Схема
молекулы воды: 1, 2, 3, 4, 5, 6, 7, 8 – номера электронов атома кислорода; P1, P2 – ядра атомов водорода (протоны); e1 и e2
–электроны атомов водорода
Таким образом, на разрушение двух молекул водорода и одной молекулы кислорода термическим
путем израсходовано 14,19эВ, а в результате синтеза двух молекул воды выделится
2,96×2=5,98эВ. В чем причина такого дисбаланса? Ответ прост. При переходе
из газообразного в жидкое состояние атом кислорода в молекуле воды, должен
уменьшить свой объём. Это произойдет, если кольцевые электроны атома кислорода
опустятся на более низкие энергетические уровни (ближе к ядру). При этом они
обязательно излучат фотоны, и мы уже знаем их общую энергию. Она равна энергии, затраченной на разрушение двух молекул водорода и одной молекулы кислорода, то
есть – 14,19эВ. Поскольку у двух молекул воды 12 кольцевых электронов, то
каждый из них излучит 14,19/12=1,18эВ. Это больше энергии (0,74эВ) связи с
ядром осевых электронов и указывает на то, что кольцевые электроны расположены
ближе к ядру, чем осевые.
В этом случае
количество энергии, полученной в результате синтеза двух молекул воды
(14,19+5,98)эВ оказывается больше энергии, затраченной на разрушение двух
молекул водорода (9,06эВ) и одной молекулы кислорода (5,13эВ). Сформировавшаяся
разность энергий 5,98эВ разделится между двумя молекулами воды. На одну
молекулу приходится (5,98/2)=2,99эВ или 285,8кДж/моль, что полностью соответствует
существующим экспериментальным данным.
Изложенное выше
проясняет причину взрыва при соединении водорода с кислородом. Одновременный
переход шести кольцевых электронов каждого атома кислорода, в рождающихся
молекулах воды, на более низкие энергетические уровни сопровождается
одновременным излучением фотонов, которые и генерируют энергию взрыва.
Обратим
внимание, что на рис.5б показано две энергии связи между валентными электронами
e2 и 2, а также между 1 и e1. Электродинамическая связь
равна 0,74эВ. Для разрыва этой связи достаточно затратить такое же количество
механической энергии. Если же эту связь облучить фотонами с энергией 0,74эВ, то
процесс поглощения фотонов будет идти так, что каждый из двух валентных
электронов поглотит по 0,37эВ и энергия связи уменьшится до 0,37эВ, и молекула
воды не разрушится. Вторая, тепловая энергия связи, указанная на том же
рисунке, равна 1,48эВ. Если оба электрона поглотят фотон с этой энергией, то
энергия связи между ними станет равной нулю и молекула воды разрушится.
Из изложенного
следует, что если указанные связи разрушать механическим путем, затрачивая по
0,74эВ на каждую связь, то после её разрыва у каждого электрона образуется
дефицит энергии, равный 0,74эВ. Эта энергия будет немедленно поглощена из
окружающей среды и излучена при повторном синтезе молекулы воды. Так
ковалентная химическая связь при механическом разрушении одной молекулы воды
формирует 1,48эВ дополнительной тепловой энергии, которая, как мы уже отметили, устойчиво регистрируется в системах кавитации воды.
Известно, что
молекулы воды, объединяясь, формируют кластеры. Если связи между молекулами в
кластерах ковалентные, то механическое разрушение этих связей также должно
сопровождаться выделением дополнительной тепловой энергии.
На Российском
рынке уже три фирмы «Юсмар», «Термовихрь» и «Нотека» продают кавитационное
водонагревательное оборудование с показателем энергетической эффективности до
150%. Готовятся к выпуску и воздушные нагревательные приборы с такой же
эффективностью. Источником дополнительной энергии, генерируемой этими
приборами, являются процессы механического разрушения ковалентных связей
молекул газов воздуха, молекул и кластеров воды, и их последующий синтез.
Заключение
Анализ
энергетического баланса молекул с ковалентными связями показывает возможность
формирования дополнительной тепловой энергии при механическом разрушении этих
связей.
Список
литературы
КанарёвФ.М.
Начала физхимии микромира. Краснодар. 2002. 320с.
Скачали данный реферат: Карюгин, Burdukovskij, Яцышин, Яркин, Ljutenkov, Paisij.
Последние просмотренные рефераты на тему: решебник 10 класс, страница реферата, контрольная работа за полугодие, изложение 6 класс.
Предыдущая страница реферата |
1
2
3
4

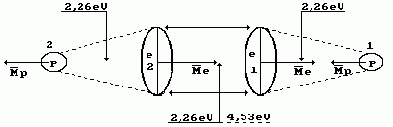

 Главная
Главная