
Эволюция биологических механизмов запасения энергии
| Категория реферата: Рефераты по науке и технике
| Теги реферата: конспект 2 класс, шпоры для студентов
| Добавил(а) на сайт: Бельтюков.
Предыдущая страница реферата | 1 2 3 4 | Следующая страница реферата
Бактериородопсин — светозависимый протонный насос. Он способен активно откачивать ионы Н1" из клетки за счет энергии видимого света, поглощенного ретиналевой частью его молекулы. В результате световая энергия превращается в трансмембранную разность электрохимических потенциалов ионов Н+ (сокращенно протонный потенциал, или ΔμΗ+). Для бактерий ΔμΗ+ — это свободная энергия ионов Н+, откачанных из клетки во внешнюю среду. Ионы Н+ как бы стремятся вернуться в клетку, где их стало меньше и где возник недостаток положительных электрических зарядов из-за действия бактериородопсинового Н+-насоса. Энергия света, запасенная таким образом в виде ΔμΗ+, освободится,
если позволить ионам Н+ войти обратно в клетку. У микробов, имеющих бактериородопсин, ионы Н4" входят через комплекс факторов F0 и F, таким образом, что освобождающаяся энергия используется для синтеза АТФ. Нетрудно представить себе, как возник фотосинтез АТФ, катализируемый бактериородопсином и комплексом F0F,. С появлением бактериородопсина клетка научилась создавать ΔμΗ+ за счет видимого света, а эта ΔμΗ+, образовавшись, просто развернула вспять Н+-АТФазную реакцию, существовавшую ранее в качестве механизма откачки из клетки гликолитических ионов Н+. Так комплекс F0F, мог превратиться из АТФазы в АТФ-синтетазу (рис. 4).
Устройство бактериородопсина намного проще
системы хлорофилльного фотосинтеза. Белковая часть бактериородопсина представляет собой одну полипептидную цепь средней длины, которая не содержит других коферментов и простетических групп, кроме ретинштя. Бактериородопсин чрезвычайно устойчив: без потери активности его можно кипятить в автоклаве при + 130°С, изменять содержание NaCl в омывающем мембрану растворе от нуля до насыщения, в широких пределах менять рН этого раствора. Более того, можно удалить выступающие из мембраны концевые участки полипептид-ной цепи и даже расщепить эту цепь в одном месте по середине без ущерба для активности насоса. В то же время эффективность бактериородопсина как преобразователя энергии сравнительно низка: всего 20% энергии светового кванта превращается в ΔμΗ+. При этом на один поглощенный квант через мембрану переносится один ион Н+.
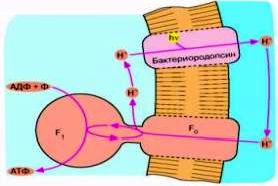
Рис. 4. Бактериородопсиновый фотосинтез со-
лелюбивых архебактерий. Ионы Н* откачиваются из клетки бактериородопсином - белком, содержащим ретиналь в качестве хромофора, то есть группировки, поглощающей видимый свет. Ионы Н* возвращаются в клетку, двигаясь "под гору" через Н*-АТФазный комплекс F0F,. При этом оказывается, что 1-Г-АТФаза катализирует обратную реакцию, то есть синтез АТФ, а не его гидролиз
Хлорофилльный фотосинтез
Хлорофилльный фотосинтез отличается от бак-териородопсинового большей эффективностью использования светового кванта. Он устроен таким образом, что либо на каждый квант переносится через мембрану не один, а два иона Н+, либо помимо транспорта Н+ происходит запасание энергии в форме углеводов, синтезируемых из СО2 и Н2О. Вот почему бактериородопсиновый фотосинтез был оттеснен эволюцией с авансцены. Он сохранился только у бактерий, живущих в экстремальных условиях, где более сложный и менее устойчивый Хлорофилльный фотосинтез, по-видимому, просто не может существовать.
Хлорофилльный фотосинтез катачизируется ферментной системой, включающей несколько белков. Квант света поглощается хлорофиллом, молекула которого, перейдя в возбужденное состояние, передает один из своих электронов в фотосинтетическую цепь переноса электронов. Эта цепь представляет собой последовательность окислительно-восстановительных ферментов и коферментов, находящихся во внутренней мембране бактерий или хлоропластов растений, где локализованы также белки, связанные с хлорофиллом. Компоненты цепи содержат, как правило, ионы металлов с переменной валентностью (железо, медь, реже марганец или никель). При этом железо может входить в состав тема (в таком случае белки называются цито-хромами). Большую роль играют также негемовые железопротеиды, где ион железа связан с белком через серу цистеина или реже азот гистидина. Помимо ионов металлов роль переносчиков электронов играют производные хинонов, такие, как убихинон, нластохинон и витамины группы К.
Перенос по цепи электрона, отнятого от возбужденного хлорофилла, завершается по-разному в зависимости от типа фотосинтеза. У зеленых бактерий, использующих комплекс хлорофилла и белка, называемый фотосистемой 1 (рис. 5, а), продуктом оказывается НАДН, то есть восстановленная форма НАД+. Восстанавливаясь, то есть присоединяя два электрона, НДЦ+ связывает также один Н+. В дальнейшем образованный таким образом НАДН окисляется, передавая свой водород на различные субстраты биосинтезов.
Что касается хлорофилла, окисленного цепью, то у зеленых серных бактерий он получит недостающий электрон от сероводорода (H2S). В результате образуются также элементарная сера и ион Н+. Белок, окисляющий H2S, расположен на внешней поверхности бактериальной мембраны, а белок, восстанавливающий НАД+, — на внутренней ее поверхности. Вот почему оказывается, что запускаемый светом перенос электронов от H,S к НАД+ образует ионы Н+ снаружи и потребляет их внутри бактерии. При этом внутренний объем клетки заряжается отрицательно относительно внешнего. Тем самым создается ДДН+, которая потребляется Н+-АТФ-синтазой (комплексом факторов F0 и FJ, образующей АТФ при переносе ионов Н "под гору", то есть снаружи внутрь.
Другой тип бактериального фотосинтеза обнаружен у пурпурных бактерий (рис, 5, б). Здесь действует набор ферментов, отличающихся от ферментного комплекса зеленых бактерий. Это несущая хлорофилл фотосистема 2 и комплекс III. Как и в предыдущем случае, процесс начинается с поглощения кванта хлорофиллом. Первоначально перенос электронов происходит по фотосистеме 2.
Затем вступает комплекс III, способный транспортировать электроны сопряженно с откачкой ионов Н+ из бактерии. Процесс завершается возвращением электрона с комплекса III на хлорофилл. Что касается ионов Н+, то они возвращаются в клетку через Н+-АТФ-синтазу, образуя АТФ.
Отличительная черта фотосинтеза у пурпурных бактерий состоит в том, что система не нуждается во внешнем доноре электронов. Откачка ионов Н* осуществляется путем циклического переноса электронов, поддерживаемого энергией света. Данное обстоятельство можно отнести, по-видимому, на счет эволюционного усовершенствования фотосинтеза пурпурными бактериями, которые по многим признакам являются эволюционно более продвинутой группой, чем зеленые серные бактерии.
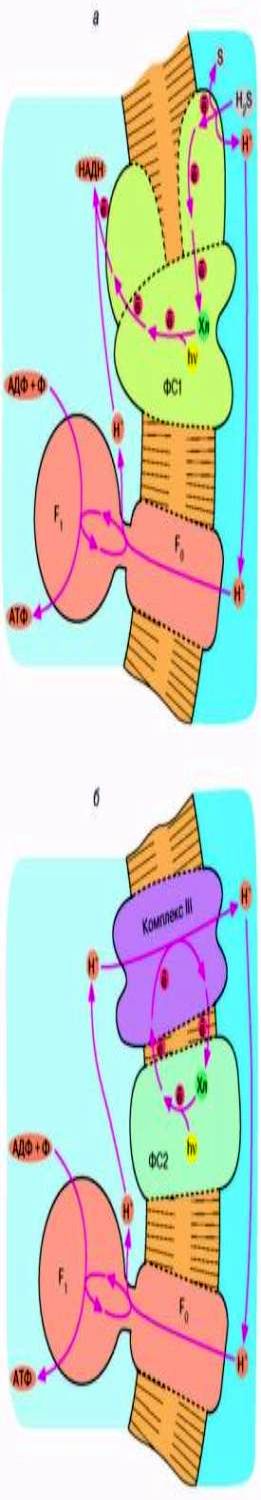
Рис. 5. Хлорофиллычый фотосинтез зеленых серных (а) и пурпурных (б) бактерий: а - хлорофилл, связанный с особым белковым комплексом - фотосистемой 1 (ФС1), возбуждается квантом света и отдает электрон по цепи электронных переносчиков на НАД*. Восстанавливаясь, НАД* связывает внутриклеточный ион Н*. Потеря электрона на хлорофилле компенсируется окислением сероводорода до серы и иона Н* снаружи бактериальной клетки. Движение Н* внутрь клетки через комплекс F0 F, дает АТФ; б - хлорофилл, связанный с белком фотосистемы 2 (ФС2), поглощает квант света и запускает циклический перенос электронов. В этом процессе участвуют переносчики электронов ФС2 и дополнительного белкового комплекса III. Перенос электронов комплексом III сопряжен с откачкой ионов Н* из клетки. Откачанные ионы Н* возвращаются через комплекс F0 F, с образованием АТФ.
Следующим шагом в эволюции фотосинтеза стали, по-видимому, цианобактерии. Цепь переноса электронов в этом случае представляет собой комбинацию: а) фотосистемы 1 зеленых бактерий, б) фотосистемы 2 и комплекса III пурпурных бактерий и в) дополнительного комплекса, расщепляющего воду на О2 и Н+ (рис. 6). Фактически донором электронов вместо сероводорода (встречающегося в достаточных количествах лишь в некоторых природных нишах) служит вездесущая вода, запасы которой практически неограничены. В результате конечный акцептор электоров — НАДФ+ восстанавливается, а вода окисляется. Образующийся НАДФН окисляется затем сложной системой восстановления углекислого газа до глюкозы. Таким образом, фотосинтез цианобактерии параллельно с образованием АТФ дает углевод — одно из главных резервных веществ современных живых клеток. Нет сомнений, что цианобактерия является эволюционным предшественником хлоропластов — органелл зеленых растений, энергетика которых устроена в основном по той же схеме, что показана на рис. 6.
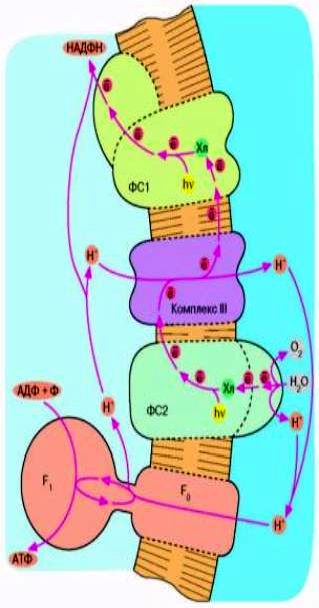
Рис. 6. Хлорофилльный фотосинтез цианобактерии. Квант света, поглощенный хлорофиллом фотосистемы 1, возбуждает перенос электронов по цепи, что завершается восстановлением НАДФ* до НАДФН. Окисленный хлорофилл фотосистемы 1 восстанавливается комплексом III, который, в свою очередь, получает электрон от фотосистемы 2. Допирование электрона фотосистемой 2 требует еще одного кванта света (поглощаемого хлорофиллом этой фотосистемы). Потеря электрона на хлорофилле фотосистемы 2 компенсируется за счет окисления молекулы воды до О2 и Н*. Ферменты, катализирующие всю цепь реакций переноса электрона от Н2О до НАДФ*, расположены в мембране таким образом, что ионы Н* откачиваются из бактериальной клетки, чтобы затем войти внутрь через F0F, и сделать АТФ. В хлоро-ппастах зеленых растений происходят те же события, но ориентация всех ферментов противоположна той, которая имеет место у цианобактерии и показана на рис. 6. Соответственно у хлоропластов фотосинтетическая цепь накачивает ионы ИГ внутрь, а комплекс F0F, переносит их наружу.
ДЫХАТЕЛЬНЫЙ МЕХАНИЗМ ЭНЕРГООБЕСПЕЧЕНИЯ.
Побочным продуктом фотосинтеза у цианобактерии и растений служит молекулярный кислород. Нарастание его концентрации в атмосфере привело к появлению ферментов, убирающих этот сильный окислитель, опасный для жизнедеятельности. Вероятно, первой функцией ферментов, восстанавливающих О, до Н2О, было снижение внутриклеточной концентрации кислорода. Однако в дальнейшем аэробная клетка научилась извлекать пользу из этого процесса, создав дыхательную цепь электронного транспорта, сопряженного с откачкой ионов Н+.
Дыхательная цепь некоторых современных бактерий включает уже знакомый нам комплекс III, служащий связующим звеном между двумя другими белковыми комплексами. Однако это уже не фотосистемы 1 и 2, а ферменты, выполняющие функции, противоположные таковым фотосистем 1 и 2. Ферменты, о которых идет речь, были названы комплекс I и комплекс ГУ.
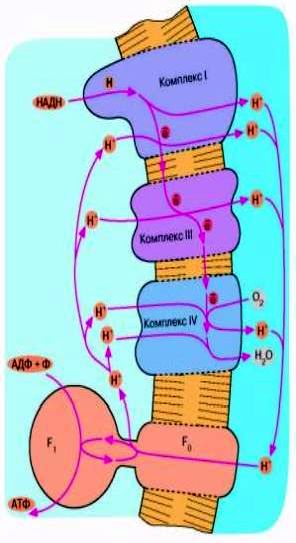
Комплекс I не восстанавливает никотинамид-ный нуклеотид, а окисляет его. Комплекс IV не окисляет воду до О2, а восстанавливает О, до воды. В итоге мы имеем сложную цепь реакций, начинающихся с окисления НАДН и кончающихся восстановлением О,. Все три комплекса дыхательной цепи способны откачивать из клетки ионы Н+ сопряженно с переносом электронов (рис, 7).
Рекомендуем скачать другие рефераты по теме: способ изложения, изложение по русскому 9 класс.
Категории:
Предыдущая страница реферата | 1 2 3 4 | Следующая страница реферата
 Главная
Главная