
Серная кислота
| Категория реферата: Рефераты по науке и технике
| Теги реферата: титульный дипломной работы, красный диплом
| Добавил(а) на сайт: Davydkin.
Предыдущая страница реферата | 1 2 3 4 5 | Следующая страница реферата
H2SO4 + 2NaOH --> Na2SO4 + 2H2O
H+ + OH- --> H2O
H2SO4 + Cu(OH)2 --> CuSO4 + 2H2O
2H+ + Cu(OH)2 --> Cu2+ + 2H2O
5) обменные реакции с солями:
BaCl2 + H2SO4 --> BaSO4 + 2HCl
Ba2+ + SO42- --> BaSO4
Образование белого осадка BaSO4 (нерастворимого в кислотах) используется для идентификации серной кислоты и растворимых сульфатов.
MgCO3 + H2SO4 --> MgSO4 + H2O + CO2 H2CO3
Моногидрат (чистая, 100%-ая серная кислота) является ионизирующим растворителем, имеющим кислотный характер. В нём хорошо растворяются сульфаты многих металлов (переходя при этом в бисульфаты), тогда как соли других кислот растворяются, как правило, лишь при возможности их сольволиза (с переводом в бисульфаты). Азотная кислота ведет себя в моногидрате как слабое основаниеHNO3 + 2 H2SO4 H3O+ + NO2+ + 2 HSO4-хлорная - как очень слабая кислотаH2SO4 + HClO4 = H3SO4+ + ClO4- Фторсульфоновая и хлорсульфоновая оказываются кислотами несколько более сильными (HSO3F > HSO3Cl > HClO4). Моногидрат хорошо растворяет многие органические вещества, имеющие в своём составе атомы с неподелёнными электронными парами (способными к присоединению протона). Некоторые из них могут быть затем выделены обратно в неизменённом состоянии путем простого разбавления раствора водой. Моногидрат обладает высоким значением криоскопической константы (6,12°) и им иногда пользуются как средой для определения молекулярных весов.
Концентрированная H2SO4 является довольно сильным окислителем, особенно при нагревании (восстанавливается обычно до SO2). Например, она окисляет HI и частично HВr (но не HСl) до свободных галогенов. Окисляются ею и многие металлы - Cu, Hg и др. (тогда как золото и платина по отношению к H2SO4 устойчивы). Так взаимодействие с медью идёт по уравнению:
Cu + 2 H2SO4 = CuSO4 + SO2 + H2O
Действуя в качестве окислителя, серная кислота обычно восстанавливается до SO2. Однако наиболее сильными восстановителями она может быть восстановлена до S и даже H2S. С сероводородом концентрированная серная кислота реагирует по уравнению:
H2SO4 + H2S = 2H2O + SO2 + S
Следует отметить, что она частично восстанавливается также газообразным водородом и поэтому не может применяться для его осушки.
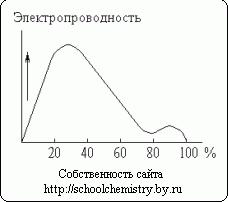
Рис. 13. Электропроводность растворов серной кислоты.
Растворение концентрированной серной кислоты в воде сопровождается значительным выделением тепла (и некоторым уменьшением общего объёма системы). Моногидрат почти не проводит электрического тока. Напротив, водные растворы серной кислоты являются хорошими проводниками. Как видно на рис. 13, максимальной электропроводностью обладает приблизительно 30 %-ная кислота. Минимум кривой соответствует гидрату состава H2SO4·H2O.
Выделение тепла при растворении моногидрата в воде составляет (в зависимости от конечной концентрации раствора) до 84 кДж/моль H2SO4. Напротив, смешиванием 66 %-ной серной кислоты, предварительно охлажденной до 0 °С, со снегом (1:1 по массе) может быть достигнуто понижение температуры, до -37 °С.
Изменение плотности водных растворов H2SO4 с её концентрацией (вес. %) дано ниже:
|
5 |
10 |
20 |
30 |
40 Рекомендуем скачать другие рефераты по теме: класс, виды шпор. Категории:Предыдущая страница реферата | 1 2 3 4 5 | Следующая страница реферата Поделитесь этой записью или добавьте в закладки |
|
 Главная
Главная