
Синтез ЖК. Дендримеры
| Категория реферата: Рефераты по науке и технике
| Теги реферата: сочинение, реферат на тему мыло
| Добавил(а) на сайт: Виссарион.
Предыдущая страница реферата | 1 2 3 4 5 6 | Следующая страница реферата
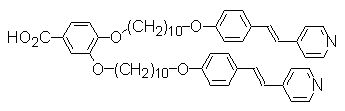
Рис. 17. АВ2-мономер, образующий гиперразветвлённые ЖК системы через водородные связи [32].
Обобщая литературные данные, следует отметить, что к настоящему времени опубликованы лишь первые работы, сообщающие о синтезе ЖК дендримеров, основанном на неуправляемом подходе. Получены только нерегулярные ЖК системы, содержащие мезогенные группы во всём объёме дендритной макромолекулы и этим напоминающие ЖК полимеры с мезогенными группами в основной цепи.
В настоящее время группой немецких исследователей ведутся работы по синтезу регулярных ЖК дендримеров методом управляемого синтеза, однако их результаты ещё не опубликованы. Поэтому данная работа и вышедшая по ней публикация [14] претендует на первенство в области синтеза регулярных ЖК дендримеров с концевыми мезогенными группами.
Синтез ЖК дендримеров
1.1. Метилсилоксановый дендример с концевыми холестеринсодержащими мезогенными группами.
На первом этапе данной работы необходимо было решить вопрос: можно ли в принципе получить дендример регулярного строения с концевыми мезогенными группами, и если да, то будет ли полученное вещество обладать ЖК свойствами. Для этого за основу была выбрана дендритная полиметилхлорсилоксановая матрица следующего строения:
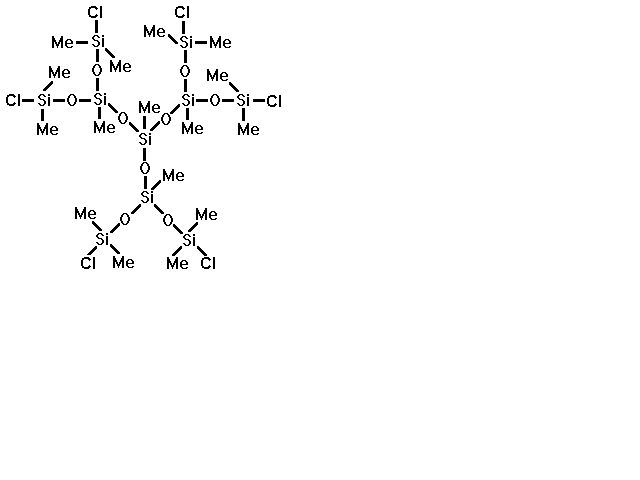
Рис.18. Исходная дендритная полиметилхлорсилоксановая матрица
Подробная методика синтеза этого соединения описана в работе [14]. Основные критерии, по которым осуществлялся выбор исходной силоксановой матрицы, заключались в синтетической доступности, простоте анализа и возможности ее выделения в индивидуальном состоянии. В рамках разработанной ранее [] методологии синтеза дендритных полиоргано-силоксанов, а также имеющихся в наличии методов анализа и выделения соединение вполне отвечает перечисленным выше критериям.
Выбранная дендритная матрица содержала концевые активные хлорсилильные группы. Для того, чтобы присоединить к ней мезогенные группы, их нужно было модифицировать таким образом, чтобы они содержали концевую группу, способную количественно заместить Si-Cl - группы выбранного дендримера с образованием стабильной связи. Силанольная группа Si-OH вполне удовлетворяет этим требованиям: она количественно реагирует с Si-Cl - группами с образованием прочной силоксановой связи. Кроме того, учитывая опыт по синтезу ЖК полимеров с мезогенными группами в боковых ответвлениях, где в качестве полимерной “матрицы” используются гребнеобразные полимеры, следует отметить, что если мезогенные группы присоединены к полимерной основе напрямую, то такие полимеры , как правило, не проявляют ЖК свойств []. Для реализации ЖК состояния в полимерах необходимо, чтобы жёсткие мезогенные группы были присоединены к основной цепи через гибкую алифатическую или другую развязку (“спейсор”). Причём ЖК свойства полимеров существенно зависят от длины этого спейсора [, ].
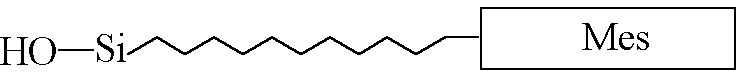
Рис.19. Схематическое изображение модифицированной мезогенной группы.
Исходя из вышесказанного, мезогенсодержащий фрагмент для “прививки” к полиметилхлорсилоксановой дендритной матрице в нашем случае должен состоять из следующих основных структурных единиц (рис. 19): мезогенной группы и алифатической развязки, содержащей концевую группу Si-OH, способную реагировать с концевыми хлорсилильными группами дендритной матрицы с образованием целевого продукта - ЖК дендримера.
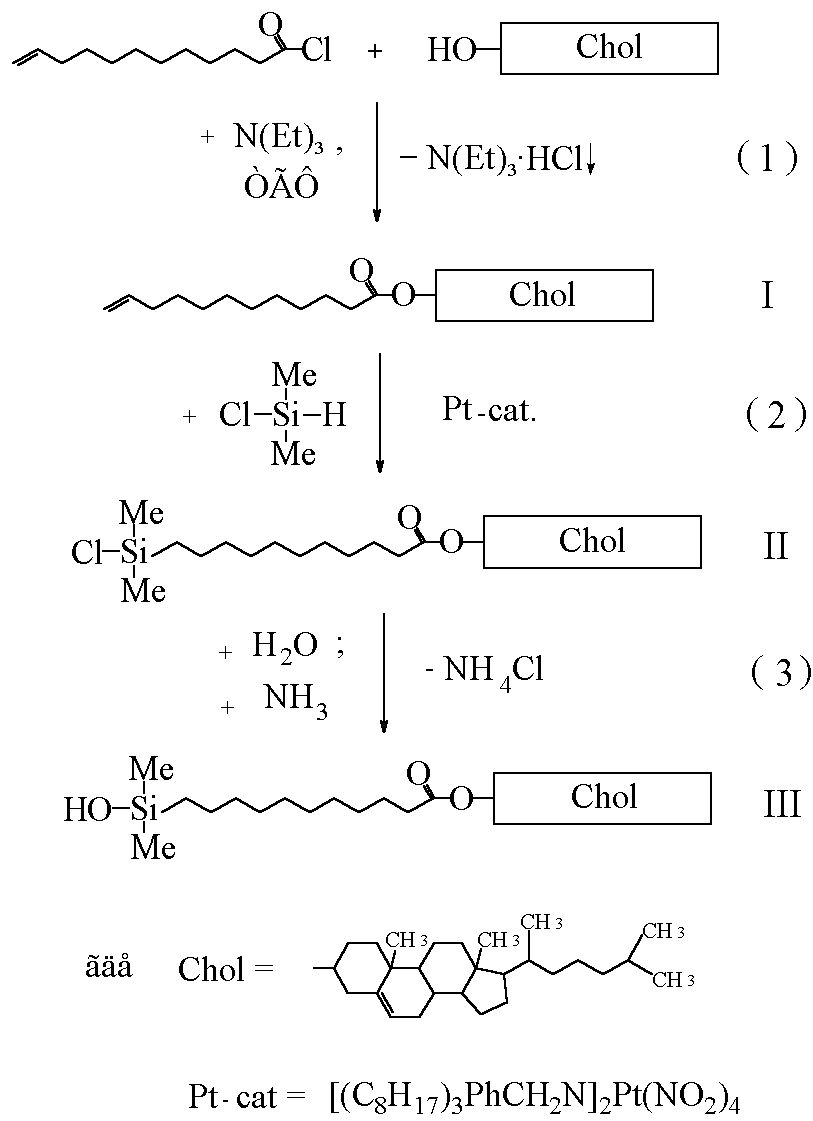
Рис.20. Схема синтеза холестеринсодержащей мезогенной группы.
В качестве мезогенной была выбрана холестериновая группа ввиду её доступности и широкого использования для синтеза гребнеобразных ЖК-полимеров. Выбор ундециленатного спейсора определялся теми же критериями.
Модификация холестериновой мезогенной группы проводилась по схеме, представленной на рис. 20.
Синтез соединения III включает в себя три химические стадии (схемы (1), (2) и (3)). Холестериновый эфир 10-ундециленовой кислоты I, был получен по стандартной методике ацилированием холестерина хлорангидридом 10-ундециленовой кислоты (схема (2)), температуры фазовых переходов совпадают с литературными данными [].
Соединение II было получено гидросилилированием эфира I в среде сухого ТГФ в присутствии трехкратного избытка диметилхлорсилана. В качестве катализатора использовали бис-(триоктилбензиламин)-тетранитрито-платину (схема (3)). Завершенность реакции контролировали методом ИК-спектроскопии (рис. 21) по исчезновению полосы валентных колебаний терминальной двойной углерод-углеродной связи в молекулах соединения I в области 1640 см-1. Одновременно наблюдали появление полосы поглощения в области 1260 см-1, соответствующей валентным колебаниям связи Si-CH3.
В спектре ПМР (Таблица 1.) образовавшегося холестеринового эфира 11-(диметилхлорсилил)-ундекановой кислоты II в отличие от исходного эфира I отсутствуют сигналы протонов, расположенных при терминальной двойной углерод-углеродной связи (дублет 1=5.2 м.д. и мультиплет 2=6.0 м.д.), что также свидетельствует о полноте протекания реакции гидросилилирования. Вместе с тем в спектре ПМР соединения II, как и в спектре соединения I, присутствуют характерные сигналы протона (3) при карбоксильной группе (мультиплет:3=4.8 м.д.) и протона (4) при двойной углерод-углеродной связи (синглет:4=5.7 м.д.) в стероидном ядре холестерила. При этом соотношение интегральных интенсивностей сигналов протонов (3) и (4) соответствует расчетному значению 1:1. Синглетный сигнал протонов метильных радикалов у атомов кремния в спектре ПМР соединения II проявляется в области =0.1 м.д. Соотношение интегральных интенсивностей сигналов протонов метильных радикалов у атомов кремния и сигналов протонов (3), (4) также соответствует расчетному значению 6:1.
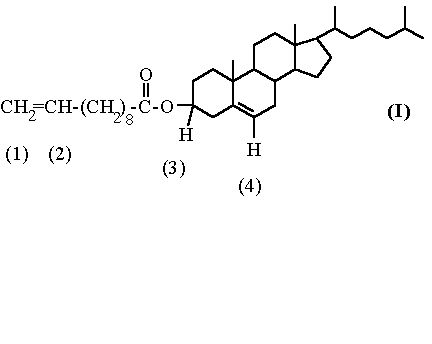
Функциональный анализ показал, что содержание хлора в полученном соединении II составляет 5.75% (расчетное значение 5.6%). Перечисленные выше данные свидетельствуют о том, что реакция гидросилилирования (схема (3)) протекает достаточно селективно по концевой двойной связи эфира I, не затрагивая двойную связь в стероидном ядре холестерина.
Гидролиз соединения II проводили в 1%-ном эфирном растворе избытком воды при 0oС, в присутствии аммиака в качестве акцептора выделяющегося HCl. Приведенные условия позволяют практически исключить протекание в реакционной системе нежелательных конденсационных процессов, приводящих к димеризации образующегося силанола III.
В ИК-спектрах силанола III наблюдается широкая полоса поглощения валентных колебаний ассоциированных гидроксильных групп у атомов кремния в области 3960 см-1.
"Прививку" холестеринсодержащих мезогенных групп к силоксановой матрице осуществляли гетерофункциональной конденсацией между и соединением III в присутствии пиридина в качестве акцептора выделяющегося HCl (рис. 22). Полученное целевое соединение IV очищали переосаждением из раствора в ТГФ этанолом. Конечный продукт представляет собой бесцветное воскообразное вещество.
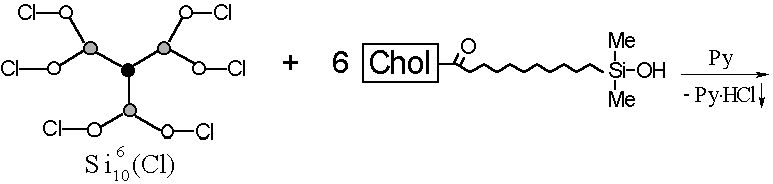
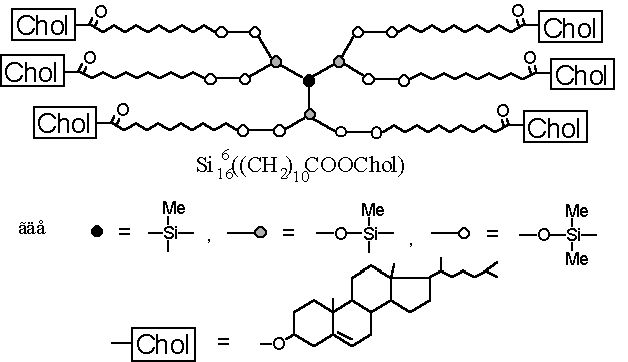
Рис.22. “Прививка” холестеринундециленатных мезогенных групп к дендритной метилхлорсилоксановой матрице.
Соотношение интегральных интенсивностей сигналов протонов метильных радикалов у атомов кремния (синглет =0.1 м.д.) в спектре ПМР соединения IV и сигналов протона при двойной углерод-углеродной связи (синглет =5.7 м.д.) в стероидном ядре холестерила близко к расчетному значению 14:1.
Кривая ГПХ соединения IV после очистки многократным переосаждением этанолом имеет вид симметричного пика (рис. 23), что также подтверждает чистоту полученного соединения.
1.2. Карбосилановые дендримеры с различными концевыми
мезогенными группами.
После того, как был получен первый дендример с концевыми холестеринсодержащими мезогенными группами было показано, что он проявляет ЖК свойства, первоочередной задачей стала разработка универсального подхода к синтезу подобных систем, позволяющего получать ЖК дендримеры на основе дендритных матриц любых размеров с различными мезогенными группами.
Схема, реализованная на первом этапе нашей работы, позволила получить первый ЖК дендример, но выход чистого конечного продукта был небольшой (20%). Очевидно, это связано с неустойчивостью при хранении промежуточного продукта - мезогенсодержащего силанола. Хотя его и удалось выделить в чистом виде и охарактеризовать, при стоянии в растворе в течении нескольких суток он практически полностью претерпевает реакцию конденсации с образованием дисилоксана. Малейшее присутствие ионных примесей катализирует этот процесс, который сам по себе не идёт. Этот недостаток значительно уменьшает привлекательность данного синтетического подхода для выбора его в качестве базовой схемы синтеза ЖК дендримеров.
Исходя из вышесказанного, на втором этапе работы мы обратили внимание на поиск иных синтетических схем для синтеза ЖК дендримеров.
Разрабатывая универсальный подход к синтезу дендримеров с концевыми мезогенными группами регулярного строения, мы принимали во внимание следующие, на наш взгляд, определяющие факторы: 1) однозначность химической реакции, позволяющая получать дендримеры со строго заданной молекулярной массой; 2) “индифферентность” химической реакции, используемой для “прививки” мезогенсодержащих фрагментов к дендритной матрице, по отношению к самой мезогенной группе.
Учитывая вышесказанное, в качестве “базовой” была выбрана реакция гидросилилирования, удовлетворяющая всем перечисленным условиям []. К настоящему времени на её основе успешно были синтезированы поликарбосилановые дендримеры [10, 11], один из которых и был взят в качестве дендритной матрицы:
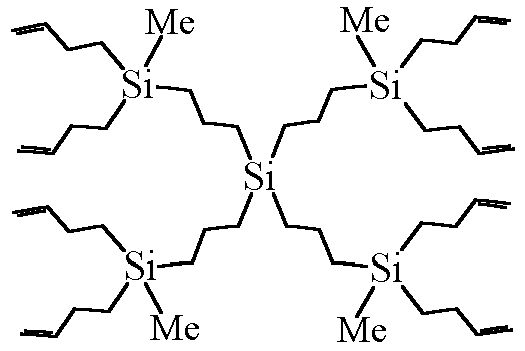
Рис.24. Исходная поликарбосилановая дендритная матрица
Подробная методика синтеза этого дендримера описана в работе [].
В нашей работе был использован поликарбосилановый дендример наименьшей генерации (G=1) по причине наибольшей его доступности, простоты выделения и идентификации конечных продуктов. Это не ограничивает универсальности разработанного синтетического подхода: по такой же схеме могут быть синтезированы ЖК дендримеры и больших генераций.
Выбранная поликарбосилановая дендритная матрица содержит концевые аллильные группы. Чтобы присоединить к ней мезогенные группы с использованием реакции гидросилилирования необходимо было их модифицировать таким образом, чтобы они содержали концевую группировку Si-H, способную реагировать с аллильными группами исходного дендримера.
Учитывая опыт по синтезу метилсилоксанового ЖК дендримера, мезогенсодержащий фрагмент для “прививки” к поликарбосилановой дендритной матрице в нашем случае должен состоять из следующих основных структурных единиц (рис. 25): мезогенной группы и алифатической развязки, содержащей концевую группу Si-H, способную реагировать с концевыми аллильными группами дендритной матрицы с образованием целевого продукта - ЖК дендримера.
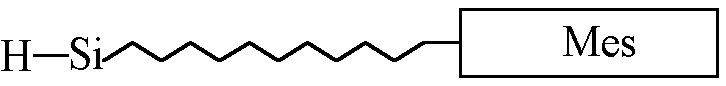
Рис.25. Схематическое изображение модифицированной мезогенной группы.
Для синтеза таких соединений нами была предложена схема, представленная на рис.9.
Рекомендуем скачать другие рефераты по теме: инновационный менеджмент, оформление курсовой работы.
Категории:
Предыдущая страница реферата | 1 2 3 4 5 6 | Следующая страница реферата
 Главная
Главная