
Химическая связь. Типы взаимодействия молекул
| Категория реферата: Биология и химия
| Теги реферата: зимой сочинение, новшество
| Добавил(а) на сайт: Федосия.
1 2 3 4 5 6 7 8 9 | Следующая страница реферата
Химическая связь. Типы взаимодействия молекул
Мельчайшей частицей вещества является молекула, образующаяся в результате взаимодействия атомов, между которыми действуют химические связи или химическая связь. Учение о химической связи составляет основу теоретической химии. Химическая связь возникает при взаимодействии двух (иногда более) атомов. Образование связи происходит с выделением энергии.
Химическая связь – это взаимодействие, которое связывает отдельные атомы в молекулы, ионы, кристаллы.
Химическая связь по своей природе едина: она имеет электростатическое происхождение. Но в разнообразных химических соединениях химическая связь бывает различного типа; наиболее важные типы химической связи – это ковалентная (неполярная, полярная), ионная, металлическая. Разновидностями этих типов связи являются донорно-акцепторная, водородная и др. Между атомами металлов возникает металлическая связь.
Химическая связь, осуществляемая за счет образования общей, или поделенной, пары или нескольких пар электронов, называется ковалентной. В образование одной общей пары электронов каждый атом вносит по одному электрону, т.е. участвует «в равной доле» (Льюис, 1916 г.). Ниже приведены схемы образования химических связей в молекулах H2, F2, NH3 и CH4. Электроны, принадлежащие различным атомам, обозначены различными символами.

В результате образования химических связей каждый из атомов в молекуле имеет устойчивую двух- и восьмиэлектронную конфигурацию.
При возникновении ковалентной связи происходит перекрывание электронных облаков атомов с образованием молекулярного электронного облака, сопровождающееся выигрышем энергии. Молекулярное электронное облако располагается между центрами обоих ядер и обладает повышенной электронной плотностью по сравнению с плотностью атомного электронного облака.

Осуществление ковалентной связи возможно лишь в случае антипараллельных спинов неспаренных электронов, принадлежащих различным атомам. При параллельных спинах электронов атомы не притягиваются, а отталкиваются: ковалентная связь не осуществляется. Метод описания химической связи, образование которой связано с общей электронной парой, называется методом валентных связей (МВС).
Основные положения МВС
Ковалентная химическая связь образуется двумя электронами с противоположно направленными спинами, причем эта электронная пара принадлежит двум атомам.
Ковалентная связь тем прочнее, чем в большей степени перекрываются взаимодействующие электронные облака.
При написании структурных формул электронные пары, обусловливающие связь, часто изображаются черточками (вместо точек, изображающих обобществленные электроны).
Важное значение имеет энергетическая характеристика химической связи. При образовании химической связи общая энергия системы (молекулы) меньше энергии составных частей (атомов), т.е. ЕAB<ЕА+ЕB.
Валентность – это свойство атома химического элемента присоединять или замещать определенное число атомов другого элемента. С этой точки зрения валентность атома проще всего определять по числу атомов водорода, образующих с ним химические связи, или числом атомов водорода, замещаемых атомом этого элемента.
С развитием квантовомеханических представлений об атоме валентность стали определять числом неспаренных электронов, участвующих в образовании химических связей. Кроме неспаренных электронов, валентность атома также зависит от числа пустых и полностью заполненных орбиталей валентного электронного слоя.
Энергия связи – это энергия, которая выделяется при образовании молекулы из атомов. Энергию связи обычно выражают в кДж/моль (или ккал/моль). Это одна из важнейших характеристик химической связи. Более устойчива та система, которая содержит меньше энергии. Известно, например, что атомы водорода стремятся объединиться в молекулу. Это означает, что система, состоящая из молекул Н2 содержит меньше энергии, чем система, состоящая из такого же числа атомов Н, но не объединенных в молекулы.
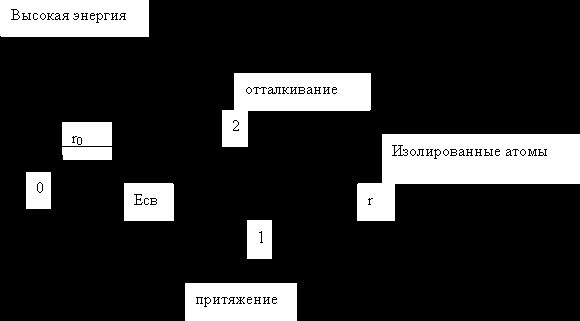
Рис. 2.1 Зависимость потенциальной энергии Е системы из двух атомов водорода от межъядерного расстояния r: 1 - при образовании химической связи; 2 – без ее образования.
На рисунке 2.1 показана энергетическая кривая, характерная для взаимодействующих атомов водорода. Сближение атомов сопровождается выделением энергии, которое будет тем больше, чем больше перекроются электронные облака. Однако в обычных условиях, вследствие кулоновского отталкивания, невозможно достичь слияния ядер двух атомов. Значит, на каком-то расстоянии вместо притяжения атомов, будет происходить их отталкивание. Таким образом, расстояние между атомами r0, которому отвечает минимум на энергетической кривой, будет соответствовать длине химической связи (кривая 1). Если же спины электронов у взаимодействующих атомов водорода одинаковы, то будет происходить их отталкивание (кривая 2). Энергия связи для различных атомов изменяется в пределах 170–420 кДж/моль (40–100 ккал/моль).
Процесс перехода электрона на более высокий энергетический подуровень или уровень (т.е. процесс возбуждения или распаривания, о котором говорилось ранее) требует затраты энергии. При образовании химической связи происходит выделение энергии. Для того, чтобы химическая связь была устойчивой, необходимо, чтобы увеличение энергии атома за счет возбуждения было меньше энергии образующейся химической связи. Иными словами, необходимо, чтобы затраты энергии на возбуждение атомов были скомпенсированы выделением энергии за счет образования связи.
Химическая связь, кроме энергии связи, характеризуется длиной, кратностью и полярностью. Для молекулы, состоящей более чем из двух атомов, существенными являются величины углов между связями и полярность молекулы в целом.
Кратность связи определяется количеством электронных пар, связывающих два атома. Так, в этане Н3С–СН3 связь между атомами углерода одинарная, в этилене Н2С=СН2 – двойная, в ацетилене НСºСН – тройная. С увеличением кратности связи увеличивается энергия связи: энергия связи С–С составляет 339 кДж/моль, С=С - 611 кДж/моль и CºC - 833 кДж/моль.
Химическая
связь между атомами обусловливается перекрыванием электронных облаков. Если
перекрывание происходит вдоль линии, соединяющей ядра атомов, то такая связь
называется сигма-связью (σ-связь). Она может быть образована за счет двух
s-электронов, s- и p-электронов, двух px-электронов, s и d электронов (например
![]() ):
):
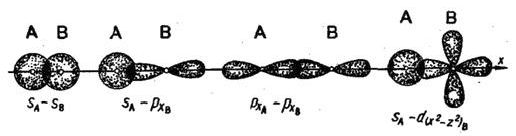
Химическая связь, осуществляемая одной электронной парой, называется одинарной. Одинарная связь – всегда σ-связь. Орбитали типа s могут образовывать только σ-связи.
Рекомендуем скачать другие рефераты по теме: ответы на сканворды в одноклассниках, реферат условия.
Категории:
1 2 3 4 5 6 7 8 9 | Следующая страница реферата
 Главная
Главная