
Химическая связь. Типы взаимодействия молекул
| Категория реферата: Биология и химия
| Теги реферата: зимой сочинение, новшество
| Добавил(а) на сайт: Федосия.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 9 | Следующая страница реферата
Волновые функции, или орбитали, водорода 1s могут дать две линейные комбинации – одну при сложении, другую - при вычитании (рис. 2.2).
Когда волновые функции складываются, то в области перекрывания плотность электронного облака, пропорциональная ψ2, становится больше, между ядрами атомов создается избыточный отрицательный заряд и ядра атомов притягиваются к нему. МО, полученная сложением волновых функций атомов водорода, называется связывающей.
Если волновые функции вычитаются, то в области между ядрами атомов плотность электронного облака становится равной нулю, электронное облако «выталкивается» из области, находящейся между атомами. Образующаяся МО не может связывать атомы и называется разрыхляющей.
Поскольку s-орбитали водорода образуют только σ-связь, то полученные МО обозначаются σcв и σр. МО, образованные 1s-атомными орбиталями, обозначаются σcв1s и σр1s.
На связывающей МО потенциальная (и полная) энергия электронов оказывается меньше, чем на АО, а на разрыхляющей – больше. По абсолютной величине возрастание энергии электронов на разрыхляющих орбиталях несколько больше уменьшения энергии на связывающих орбиталях. Электрон, находящийся на связывающих орбиталях, обеспечивает связь между атомами, стабилизируя молекулу, а электрон на разрыхляющей орбитали дестабилизирует молекулу, т.е. связь между атомами ослабевает. Еразр. > Есв.
МО образуются и из 2р-орбиталей одинаковой симметрии: связывающая и разрыхляющая σ-орбитали из 2р-орбиталей, расположенных по оси х. Они обозначаются σcв2р и σр2р. Связывающая и разрыхляющая p-орбитали образуются из 2рz-орбиталей. Обозначаются они соответственно πсв2рz, πp2pz. Аналогично образуются πсв2ру и πр2ру-орбитали.
Заполнение МО. Заполнение МО электронами происходит в порядке увеличения энергии орбиталей. В случае, если МО имеют одинаковую энергию (πсв- или πр-орбитали), то заполнение происходит по правилу Хунда так, чтобы спиновый момент молекулы был наибольшим. Каждая МО, как и атомная, может вместить два электрона. Как отмечалось, магнитные свойства атомов или молекул зависят от наличия неспаренных электронов: если в молекуле есть неспаренные электроны, то она парамагнитна, если нет – диамагнитна.
Рассмотрим
ион ![]() .
.
Из
схемы видно, что единственный электрон размещается по σcв - МО. Образуется
устойчивое соединение с энергией связи 255 кДж/моль, длиной связи - 0,106 нм.
Молекулярный ион ![]() парамагнитен. Если принять, что кратность
связи, как в методе ВС, определяется количеством электронных пар, то кратность
связи в
парамагнитен. Если принять, что кратность
связи, как в методе ВС, определяется количеством электронных пар, то кратность
связи в ![]() равна ½. Записать процесс образования
равна ½. Записать процесс образования ![]() можно следующим образом:
можно следующим образом:
![]() .
.
Эта запись означает, что на σcв МО, образованной из 1s АО, находится один электрон.
Молекула
обычного водорода содержит уже два электрона с противоположными спинами на
σcв1s-орбитали: ![]() . Энергия
связи в Н2 больше, чем в
. Энергия
связи в Н2 больше, чем в ![]() - 435 кДж/моль, а длина связи (0,074 нм) –
меньше. В молекуле Н2 имеется одинарная связь, молекула диамагнитна.
- 435 кДж/моль, а длина связи (0,074 нм) –
меньше. В молекуле Н2 имеется одинарная связь, молекула диамагнитна.
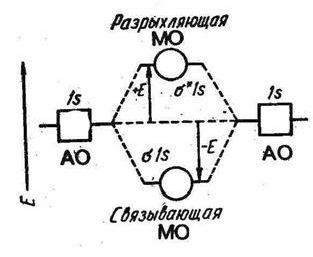
Рис. 2.3. Энергетическая диаграмма АО и МО в системе их двух атомов водорода.
Молекулярный
ион ![]() ([He[1s2]+He+[1s1] ® He+2[(sсв1s)2(sр1s)1])
имеет уже один электрон на σразр.1s-орбитали. Энергия связи в
([He[1s2]+He+[1s1] ® He+2[(sсв1s)2(sр1s)1])
имеет уже один электрон на σразр.1s-орбитали. Энергия связи в ![]() - 238 кДж/моль (по сравнению с Н2 понижена), а
длина связи (0,108 нам) - увеличена. Кратность связи равна ½ (кратность
связи равна половине разности числа электронов на связывающих и разрыхляющих
орбиталях).
- 238 кДж/моль (по сравнению с Н2 понижена), а
длина связи (0,108 нам) - увеличена. Кратность связи равна ½ (кратность
связи равна половине разности числа электронов на связывающих и разрыхляющих
орбиталях).
|
Li2 |
(Be)2 |
B2 |
N2 |
O2 |
(Ne)2 |
CO |
NO |
|
|
σp2px |
– Рекомендуем скачать другие рефераты по теме: ответы на сканворды в одноклассниках, реферат условия. Категории:Предыдущая страница реферата | 1 2 3 4 5 6 7 8 9 | Следующая страница реферата Поделитесь этой записью или добавьте в закладки |
|
 Главная
Главная