|
Cd2+ + 2H2O = Cd(OH)2o
+ 2H+
|
log 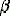 -2,1,0
= - 20.38 -2,1,0
= - 20.38
|
|
2Cd2+ + H2O
= Cd2(OH)3+ + H+
|
log 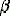 -1,2,0
= - 9.36 -1,2,0
= - 9.36
|
|
Cd2+ + 2H2O = 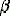 -Cd(OH)2 (тв) + 2H+ -Cd(OH)2 (тв) + 2H+
|
log 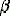 Cd = -
13,68 Cd = -
13,68
|
|
Fe3+ + H2O
= Fe(OH)2+ + H+
|
log 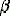 -1,0,1
= - 2.25 -1,0,1
= - 2.25
|
|
Fe3+ + 2H2O
= Fe(OH)2+ + 2H+
|
log 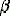 -2,0,1
= - 5.76 -2,0,1
= - 5.76
|
|
Fe3+ + 3H2O = Fe(OH)3o
+ 3H+
|
log 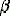 -3,0,1
= - 12.09 -3,0,1
= - 12.09
|
|
Fe3+ + 4H2O
= Fe(OH)4- + 4H+
|
log 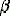 -4,0,1
= - 21.66 -4,0,1
= - 21.66
|
|
Fe3+ + 1.5H2O
= 0.5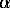 -Fe2O3
+ 3H+ -Fe2O3
+ 3H+
|
log 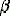 Fe =
0.61 Fe =
0.61
|
Константы
поверхностных равновесий, определенные уравнениями (1) и (2), являются
кажущимися, поскольку зависят от заряда поверхности. Для получения истинных
констант они должны быть ?исправлены¦ на кулоновскую энергию заряженной
поверхности:
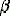 sp,0,0 (int) =
sp,0,0 (int) =
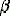 sp,0,0 exp (pF
sp,0,0 exp (pF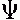 /RT) , (10)
/RT) , (10)
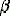 spp (int) =
spp (int) = 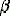 spp exp((p-1)F
spp exp((p-1)F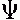 /RT) (11)
/RT) (11)
где
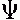 -
электростатический потенциал поверхности, F - число Фарадея.
-
электростатический потенциал поверхности, F - число Фарадея.
Балансовые
уравнения для H+(H),  FeOH (B), Cd2+
(Cd), адсорбированного Cd (Cdads) и Fe3+ (D) записаны
ниже в виде уравнений (12) - (15):
FeOH (B), Cd2+
(Cd), адсорбированного Cd (Cdads) и Fe3+ (D) записаны
ниже в виде уравнений (12) - (15):
TOT(H)
= [H+] - [OH-] - 2[Cd(OH)2 s] + 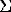 p[Hp(--O-FeOH)p]
+
p[Hp(--O-FeOH)p]
+ 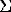 p[Hp(--OH-CdOH)p-1]
+
p[Hp(--OH-CdOH)p-1]
+ 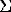 p[HpCdrp+2r]
+
p[HpCdrp+2r]
+ 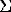 (p+3)[HpFesp+3s]
(12)
(p+3)[HpFesp+3s]
(12)
TOT(B) =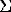 [Hp(--O-FeOH)p]
+
[Hp(--O-FeOH)p]
+ 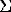 [Hp(--OH-CdOH)p-1]
(13)
[Hp(--OH-CdOH)p-1]
(13)
TOT(Cd) = [Cd2+] + 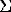 r[HpCdrp+2r]
+
r[HpCdrp+2r]
+ 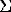 [Hp(-OH-CdOH)p-1]
+ [Cd(OH)2 ] (14)
[Hp(-OH-CdOH)p-1]
+ [Cd(OH)2 ] (14)
TOT(D) - TOT(B) = [Fe3+]
+ 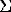 s[HpFesp+3s]
+ 0.5[Fe2O3 s] -
s[HpFesp+3s]
+ 0.5[Fe2O3 s] - 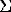 [Hp(--OH-CdOH)p-1]
, (15)
[Hp(--OH-CdOH)p-1]
, (15)
Рекомендуем скачать другие рефераты по теме: характер реферат, шпаргалки на телефон.
Предыдущая страница реферата |
1
2
3
4
5
6
7
8 |
Следующая страница реферата
 Главная
Главная