
Адсорбция и поверхностное осаждение кадмия на гематите
| Категория реферата: Рефераты по экологии
| Теги реферата: бесплатные конспекты, цивилизация реферат
| Добавил(а) на сайт: Pustov.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата
|
Комбинация комплексов |
log |
V(Y) |
log |
V(Y) |
|
--OH-CdOH |
-12.14 ± 0.02 |
70 |
-12.02 ± 0.03 |
33 |
|
--OH-CdOH2+ |
-3.07 ± 0.03 |
31 |
-3.12 ± 0.03 |
17 |
|
--OH-CdOH2+ --OH-CdOH |
-3.28 ± 0.03 -13.10 ± 0.05 |
16 |
-3.23 ± 0.03 -13.09 ± 0.07 |
7 |
|
--OH-CdOH2+ --OH-CdO- |
-3.17 ± 0.02 -22.96 ± 0.08 |
19 |
-3.22 ± 0.03 -22.94 ± 0.12 |
9 |
При всех других возможных комбинациях комплексов сходимость при оптимизации параметров отсутствует.
К наилучшему согласию с экспериментальными данными приводят две модели, включающие по два поверхностных комплекса --OH-CdOH2+ + --OH-CdOH (22, 23) и OH-CdOH2+ + --OH-CdO- (22, 24) в соответствии со следующими равновесиями:
--O-FeOH + Cd2+ + 2H+
--OH-CdOH2+ + Fe3+, ![]() sp2 (22)
sp2 (22)
--O-FeOH + Cd2+ + H+
--OH-CdOH + Fe3+ , ![]() sp1 (23)
sp1 (23)
--O-FeOH + Cd2+
--OH-CdO- + Fe3+ . ![]() sp0
(24)
sp0
(24)
Предпочесть какую-либо из этих двух моделей невозможно на основании полученных результатов, поскольку критерий V(Y) практически одинаков (см. Табл. 3). Таким образом, в данном случае мы сталкиваемся с ситуацией, когда термодинамическое моделирование не в состоянии обеспечить выбор наиболее достоверной модели с определенным набором поверхностных комплексов. Сомнительно также, что в данном случае картину смогут уточнить электрокинетические данные (например, по электрофорезу), поскольку обе модели дают практически идентичное описание pH-зависимости заряда (и потенциала) поверхности. Для получения информации о реакциях протонирования на молекулярном уровне необходимы такие дополнительные методы, как ИК Фурье-спектроскопия [24].
Результаты термодинамического моделирования показаны на рис. 1., где представлены экспериментальные и расчетные данные общей концентрации для Cdads и протона.
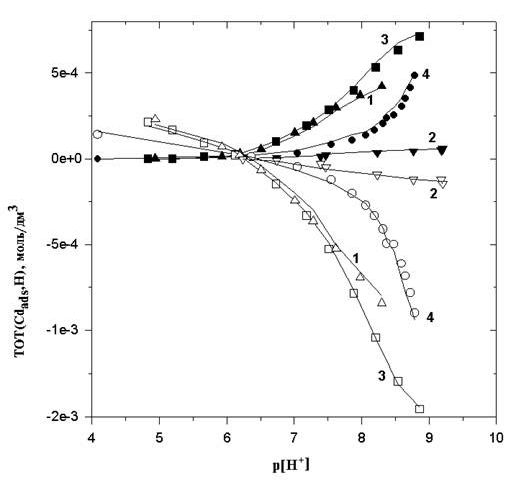
Рис. 1. Общая концентрация сорбированного кадмия (закрашенные символы) и протона в зависимости от p[H+]. Линии - расчет по модели с поверхностными комплексами --OH-CdOH2+ и --OH-CdOH (см. Табл. 3). TOT(Cd)/TOT(B) = 0,56 (1); 0,78 (2); 1,00 (3); 3.80 (4).
Привлекает внимание возможность выбора модели с одним поверхностным комплексом --OH-CdOH2+. Действительно, если рассматривать данные только по адсорбции кадмия, такая модель была бы приемлема и вследствие своей простоты предпочтительна, однако совместное описание адсорбции кадмия и протона с помощью этой модели существенно хуже (см. Табл. 3).
Сравним
полученную модель с моделями других авторов, в частности [3] и [8, 12]. Это
интересно сделать, так как мы использовали экспериментальные и теоретические
подходы, элементы которых можно встретить именно в этих работах. Авторы [3] при
изучении сорбции кадмия на гетите, так же как и мы, использовали комбинацию
кислотно-основного потенциометрического титрования и адсорбционных измерений; в
расчетах также использовали модель постоянной емкости и наилучшее согласие с
экспериментальными данными получили в модели с тремя поверхностными
комплексами: ![]() FeOCd+,
FeOCd+, ![]() FeOHCd2+
и
FeOHCd2+
и ![]() FeOCdOH. В
этой работе при отношении общей концентрации кадмия к общей концентрации
адсорбционных центров больше единицы наблюдалось значительное расхождение
экспериментальных данных и расчета в той области рН, где еще не достигалось
произведение растворимости кадмия, но концентрация адсорбированного кадмия уже
превышала величину предельной адсорбции. Очевидно, что любая модель
поверхностного комплексообразования в принципе не способна описывать данные в
той области, где уже произошло насыщение адсорбционных центров, и наблюдается
дальнейшее снижение концентрации кадмия в растворе.
FeOCdOH. В
этой работе при отношении общей концентрации кадмия к общей концентрации
адсорбционных центров больше единицы наблюдалось значительное расхождение
экспериментальных данных и расчета в той области рН, где еще не достигалось
произведение растворимости кадмия, но концентрация адсорбированного кадмия уже
превышала величину предельной адсорбции. Очевидно, что любая модель
поверхностного комплексообразования в принципе не способна описывать данные в
той области, где уже произошло насыщение адсорбционных центров, и наблюдается
дальнейшее снижение концентрации кадмия в растворе.
В
работах Мореля с сотрудниками [8,15] впервые предложена модель поверхностного
осаждения, удовлетворительно описывающая сорбцию, включая переходную область
между адсорбцией (поверхностным комплексообразованием) и объемным осаждением
гидроксида металла. При рассмотрении процесса поверхностного осаждения авторы
изменяют вид реакций адсорбции таким образом, что при взаимодействии иона
металла с адсорбционным центром ![]() FeOH
образуется новая функциональная группа =MeOH2+, на
которой происходит дальнейшая адсорбция Me2+ с образованием Me(OH)2.
FeOH
образуется новая функциональная группа =MeOH2+, на
которой происходит дальнейшая адсорбция Me2+ с образованием Me(OH)2.
В этой работе a priori постулируется модель с одним типом поверхностного комплекса =MeOH2+. Авторы не используют однако в расчетах данные по адсорбции протона; действительно, из наших результатов также видно (Табл. 3), что при обработке данных только по кадмию модель с одним поверхностным комплексом может рассматриваться как удовлетворительная, что нельзя сказать в случае совместного описания адсорбции кадмия и протона.
Использованный в настоящей работе подход в значительной степени свободен от недостатков, перечисленных выше. Он позволяет удовлетворительно описывать данные по кадмию и протону во всем интервале pH и концентрации Cd, включая переходную область от поверхностного комплексообразования к объемному осаждению Cd(OH)2(s).
Модель поверхностного осаждения - единственная на сегодняшний день модель, позволяющая количественно описать осаждение твердой фазы из ненасыщенного раствора. Основой этой модели является предположение об образовании идеального твердого раствора (гидр)оксида сорбирующегося металла и сорбента (субстрата). Реальность образования двойных гидроксидов при сорбции металлов (Co, Ni, Mg, Zn) на (гидр)оксидах, силикатах и глинистых минералах доказана прямыми спектроскопическими наблюдениями [17,18,19]. Что касается идеальности образующегося твердого раствора, то это, конечно, существенное упрощение, позволяющее осуществить количественное описание образования твердого раствора.
Широко распространенным в природе механизмом образования твердой фазы является гетерогенное зародышеобразование [22]. Аналогично тому, как катализаторы снижают энергию активации химической реакции, присутствие другой твердой фазы уменьшает энергетический барьер для зародышеобразования. Однако пока раствор ненасыщен, образующиеся зародыши новой фазы являются нестабильными, если только отсутствуют какие-либо механизмы, снижающие активность осаждающегося вещества. Таким механизмом и может быть образование твердого раствора, что учитывается моделью поверхностного осаждения.
Список литературы
1. Schwertmann, U., Cornell, R. M. Iron Oxides in the Laboratory. Weinheim: VCH Verlagsges. 1991. 132 P.
2. Moore J.W., Ramamoorthy S. Heavy metals in natural waters. NY: Springer, 1983. 268 P.
Рекомендуем скачать другие рефераты по теме: характер реферат, шпаргалки на телефон.
Категории:
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата
 Главная
Главная