
Математика в химии и экономике
| Категория реферата: Рефераты по математике
| Теги реферата: доклад на тему, инвестиции реферат
| Добавил(а) на сайт: Летов.
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата
2/3 c1+1/3 c3=0,8c1 ,
2/3 c2+1/3 c3=1,1c2 ,
или
2c1 -5c3 =0 ,
13c2 -10c3=0 .
Из этой системы, так же как и в предыдущей задаче нельзя определить все три концентрации с1, c2 и c3. Но благодаря тому, что уравнения системы представляют собой однородные линейные выражения, из нее можно найти отношения двух концентраций к третьей например, с1/с3 и с2/с3:
m=с1/с3=5/2 , n=с2/с3=10/13 .
Количество спирта в первой пробирке относится к количеству спирта во второй пробирке, как m/n. Действительно,
V0с1/V0с2=m/n=13/4 .
Поэтому ответ в данной задаче такой: 13:4.
Обратимся теперь к задачам, которые можно объединить в одну группу из-за того, что их решение связано с выявлением общей закономерности изменения той или иной величины в результате многократно повторяющейся операции.
Рассмотрим следующий пример.
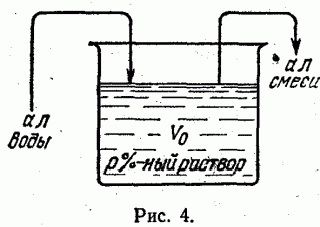
Задача 3. В сосуде, объем которого равен V0 л, содержится р%-ный раствор соли (рис. 4). Из сосуда выливается, a л смеси и доливается а л воды, после чего раствор перемешивается. Эта процедура повторяется n раз. Спрашивается, по какому закону меняется концентрация соли в сосуде, т.е. какова будет концентрация соли после n процедур?
Решение. Очевидно, что первоначальное количество соли в растворе равно
p/100 x V0 .
После того как отлили а л смеси, в растворе осталось
p/100 x V0 - p/100 x a = p/100 x V0 (1-a/V0)
соли, а ее концентрация после добавления а л воды стала равной
c1 = p/100 х (1-a/V0) .
После того как отлили еще а л смеси (но уже с концентрацией c1), в растворе осталось соли
1/100 х V0 (1-a/V0)-c1a= p/100 х V0 (1-a/V0)2 ,
а ее концентрация после добавления а л воды стала равной
c2=p/100 х (1-a/V0)2 .
Нет надобности еще раз проделывать ту же процедуру, чтобы убедиться, что концентрация соли в растворе после n переливаний определяется формулой
Рекомендуем скачать другие рефераты по теме: оформление доклада, онегин сочинение.
Категории:
Предыдущая страница реферата | 1 2 3 4 5 6 7 8 | Следующая страница реферата
 Главная
Главная